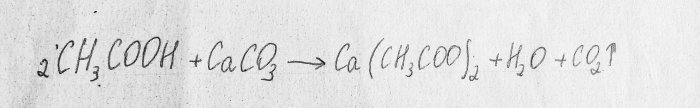En integrerad del av varje lång resa är en bål. Turister använder ofta torrt bränsle för snabb tändning. Men om en turistkemist går på vandring, finns det i hans arsenal för antändning något mer intressant - fast alkohol. Det ser ut så här:
Det kommer att diskuteras i den här artikeln. Jag noterar att bara namnet kombinerar detta ämne med alkohol - vi kommer att verifiera det senare. Låt oss nu laga det!
Kommer att behöva
Som kemiska reagens använder vi det som lätt kan hittas i hyllorna.
Så för beredningen av fast alkohol behöver vi:
- Ättiksyra 70%, säljs i livsmedelsbutiker;
- Naturlig krita - i butiker för en sommarresidens;
- Medicinsk alkohol 95% eller isopropylalkohol - på ett apotek respektive i en bilbutik.
Vi behöver också några vatten- och engångsrätter för själva experimentet och gummihandskar. Använd aldrig något av ovanstående för mat efter att ha avslutat experimenten!
Som en mätkopp kan du använda en 200 ml plastkopp.
Låt oss börja göra torr alkohol
Tillsätt först 60 ml ättiksyra och 125 ml vatten i kolven.
Nu lägger vi krita i små portioner till den resulterande lösningen. Gasbubblor börjar stå ut, medan det är viktigt att hela tiden röra lösningen så att de har tid att spricka.
Den totala konsumtionen av krita är 42 gram, men den bör tillsättas tills den upphör att lösa upp.
Tänk på processens kemiska reaktion:
Detta är en neutraliseringsreaktion.
Den första substansen är ättiksyra. Den andra är kalciumkarbonat, som finns i krita. Resultatet av denna reaktion är koldioxid, vatten och kalciumacetat. Detta ämne är dåligt lösligt i vatten, så under experimentet kan lösningen härda framför ögonen:
I det här fallet måste du lägga till lite vatten och fortsätta experimentet.
När syran inte förblir i lösningen kommer reaktionen att upphöra. Låt honom stå stilla.
Efter en tid kommer överskott av krita att sätta sig till botten, eftersom det i sig själv är olösligt i vatten. Filtrera nu lösningen:
Jag använde ett pappersfilter, du kan också använda en bomullsdyna.
Den filtrerade lösningen har en gulaktig nyans; det är en mer eller mindre ren lösning av kalciumacetat. Häll en liten mängd i en annan behållare och häll lite alkohol. En geléliknande massa börjar bildas:
Eller en ljusare nyans:
Grattis, vi fick den hårda alkoholen! I själva verket började kalciumacetat, på grund av närvaron av alkohol, som vi tillsatte, utfällas i form av monohydrat; för alkohol tenderar att förskjuta salterna av tvåvärda metaller från lösningen, som vi observerar.
Nu med våra händer (alltid handskar!) Vi ger vår gelé formen av en kub eller en boll.
Vid en temperatur på 160 grader sönderdelas kalciumacetat, i synnerhet - till lätt brännbara ämnen, vilket bidrar till ytterligare sönderdelning och stödjer lågan.
En bit av denna storlek kan brinna upp till sex minuter, vilket är ett ganska bra resultat. Och två bitar räcker för att göra te för en person. Som ett resultat av experimentet erhölls en tillräcklig mängd kalciumacetat, vilket betyder att det kommer att pågå under lång tid.
slutsats
Efter tillverkningen placerar vi den fasta alkoholen i önskad form i en hermetiskt förseglad behållare och dristig tar den med oss på en campingtur. Och på detta slutade den här artikeln. Ha en trevlig resa!
P.S.Dessutom kan färglösa nålformade kristaller odlas av kalciumacetat, men det här är en helt annan historia ...