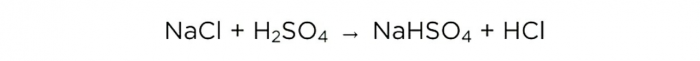Alchemicy, którzy po raz pierwszy otrzymali kwas chlorowodorowy w XV wieku, nazwali go „spiritus salis”, „duchem z soli”. Kwas ten miał wówczas magiczne właściwości: powodował korozję papieru, rozpuszczał metale, zatruwał ludzi. Te właściwości pozostały z nią do dnia dzisiejszego, ale teraz ten kwas został wystarczająco zbadany i nie ma tu magii.
Kwas solny (HCl) jest silnym kwasem jednozasadowym, w czystej postaci jest przezroczystą cieczą. Przy maksymalnym stężeniu 38% „pali” w powietrzu. Otrzymamy kwas o stężeniu równym połowie tego.
Więc zacznijmy.
Środki ostrożności
Uwaga, pracuj z substancjami toksycznymi!
Wszystkie eksperymenty muszą być przeprowadzane w dobrze wentylowanym pomieszczeniu lub pod wyciągiem. Pamiętaj, aby nosić okulary ochronne (dostępne w sklepie. Sklep) i rękawiczki (jeśli nie znajdziesz specjalnych rękawic chemicznych, są one dobrej jakości do mycia naczyń).
W miejscu eksperymentu musi być obecna soda oczyszczona, aby zneutralizować kwas w nieprzewidzianej sytuacji (uwolniony zostanie dwutlenek węgla i woda).
Surowo zabrania się przeprowadzania eksperymentu w metalowych pojemnikach.
Będzie potrzebować
Do przeprowadzenia eksperymentu potrzebujemy:
- Kwasowy elektrolit do akumulatorów (sprzedawany w sklepie samochodowym);
- Woda destylowana (ibid.);
- Sól (jest w dowolnej kuchni);
- Soda oczyszczona (patrz środki ostrożności).
Z naczyń potrzebujesz:
- Szklana kolba;
- Naczynie z piaskiem, w którym można umieścić kolbę;
- Kilka kubków jednorazowych o pojemności 200 ml;
Jeśli masz żaroodporną żarówkę, możesz ją podgrzać pod otwartym płomieniem palnika. Ale nadal polecam przez piasek, w którym to przypadku wchłania kwas.
Będziesz także potrzebował pary narożników hydraulicznych o średnicy 50 mm i palnika (w moim przypadku alkoholu, ale zalecam użycie gazowego).
Etap 1 - odparowanie
Elektrolit akumulatorowy jest najbardziej 36% kwasem siarkowym (H2SO4). Po pierwsze, musimy zwiększyć jego koncentrację.
Wlać 200 ml do szklanki, czyli prawie do krawędzi i wlać nieco więcej niż połowę szklanki do kolby. Zrób znacznik ze znacznikiem i dodaj resztę.
Wstawiłem odbłyśnik foliowy wokół kolby w celu wydajniejszego ogrzewania, ale później ją usunąłem, ponieważ zaczął się topić.
Teraz kładziemy kolbę na palniku i odparowujemy do poziomu wcześniej ustawionego znaku, nawet nieco niższego.
Równolegle kładziemy gazę złożoną kilka razy nad rogiem i mocujemy za pomocą elastycznej taśmy. Przygotowujemy nienasycony roztwór sody i zanurzamy w nim koniec rogu gazą.
Kiedy elektrolit zacznie wrzeć, kładziemy róg na kolbie, która mocno przylega do niej. Koniec z gazy jest wysyłany do otwartego okna.
Jest to konieczne, jeśli nagle sam kwas siarkowy zaczyna odparowywać z wodą. Jeśli nie przegrzejesz zbytnio kolby, tak się nie stanie.
Palnik w akcji:
Moc mojego palnika jest stosunkowo niewielka, więc odparowanie zajęło około godziny. Palnik gazowy lub kuchenka elektryczna znacznie przyspieszy ten proces.
Po zakończeniu pierwszego etapu w kolbie powinna pozostać nieco mniej niż połowa roztworu, tj. Kwas o stężeniu około 75%. Nie zapomnij o dokładności.
Niech ostygnie do temperatury pokojowej.
Etap 2 - obliczenia
Teraz, gdy skoncentrowaliśmy kwas siarkowy, możemy przeprowadzić główną reakcję, wygląda to następująco:
Ale najpierw wykonajmy obliczenia, a na koniec porównamy je z tym, co wydarzyło się w praktyce.
Tak więc początkowo mieliśmy 200 ml elektrolitu o gęstości 1,27 g / cm³. Patrząc na tabelę gęstości kwasu siarkowego, widzimy, że gęstość ta odpowiada stężeniu 36%. Obliczyć objętość kwasu:
200 ml * 36% = 72 ml - V (H2SO4)
Po odparowaniu roztworu jego stężenie i odpowiednio gęstość wzrosły. Patrzymy na tę samą tabelę i widzimy, że stężenie 75% odpowiada gęstości 1,67 g / cm³.
Znając gęstość prądu (p) i objętość (V) kwasu, uzyskujemy masę:
m = p * V;
m (H2SO4) = 1,67 g / cm3 * 72 ml = 120 g;
m (H2SO4) = 1,67 g / cm3 * 72 ml = 120 g;
Teraz ze szkolnej chemii przypominamy:
m (H2SO4) / M (H2SO4) = m (NaCl) / M (NaCl) = m (HCl) / M (HCl),
gdzie M jest masą molową substancji.
gdzie M jest masą molową substancji.
Masy molowe H2SO4, NaCl i HCl wynoszą odpowiednio 98, 58,5 i 36,5 g / mol. Teraz możemy dowiedzieć się, ile soli jest potrzebne i ile HCl będzie.
Mianowicie potrzebujemy 72 g NaCl, to jest 34 ml, weź w nadmiarze - ćwierć szklanki.
Doskonały, a HCl w teorii wyniesie 44,7 g.
W tabeli gęstości HCl znajduje się kolumna g / l. Bierzemy stąd wartość stężenia 15% - 166,4 g / l. Objętość wody wymagana do uzyskania 15% HCl wynosi 44,7 / 166,4≈270 ml. Weźmiemy 200 ml. W rezultacie otrzymam w teorii 22% kwas solny.
Etap 3 - uzyskanie kwasu
Łączymy dwa rogi w następujący sposób:
A cała struktura będzie wyglądać następująco:
Odpowiedni kwas skropli się w naczyniu oznaczonym HCl, objętość w nim wody wynosi 200 ml. Zaznacz także bieżący poziom płynu na tym naczyniu.
Usuwamy rogi i wlewamy ilość soli obliczoną w obliczeniach do kolby przez lejek.
Roztwór zmienia kolor na żółty.
Aby kwas chlorowodorowy zaczął się wyróżniać, musisz włączyć palnik. Ale najpierw mocno przymocowujemy rogi do kolby i naczynia odbierającego.
W wyniku kondensacji kwasu w wodzie powstają „fale pionowe”. Ponadto roztwór nagrzewa się i musi zostać schłodzony. Na przykład możesz postawić inny statek z lodem od dołu.
Reakcja przebiega stosunkowo szybko - 20 minut, po których można wyłączyć ogień. Dajemy ostatnie pary kwasu solnego do rozpuszczenia w wodzie, po czym szczelnie zamykamy naczynie. Po schłodzeniu kolby rozcieńczamy pozostały roztwór wodą (około jeden do jednego) i wlewamy do kanalizacji.
Podsumowanie
Na podstawie etykiety na naczyniu określamy, ile płynu zostało dodane. Mam to ⅙, czyli 17%. To jest stężenie naszego kwasu solnego. Porównaj to z uzyskanym teoretycznie.
17% / 22% * 100% = 77% to wydajność reakcji.
Ważne jest, aby pamiętać, że nie ma wyjścia równego 1, zawsze są straty. W moim przypadku nie wystarcza odparowany elektrolit. Idealnie stężenie kwasu siarkowego powinno wynosić 90-95%.
Sprawdź powstały kwas pod kątem interakcji z metalem.
Obserwujemy szybką ewolucję wodoru. Oznacza to, że kwas jest odpowiedni do dalszych eksperymentów.
Wariacje
Jako kolbę możesz użyć czystej szklanej butelki piwa lub sody, ale pod warunkiem, że ogrzewanie jest tak płynne, jak to możliwe. Zamiast narożników z PCV możesz wziąć rury polipropylenowe i narożniki o mniejszej średnicy (odpowiednie dla twojej kolby).
Jeszcze raz wzywam do przestrzegania zasad bezpieczeństwa. Powodzenia wszystkim!