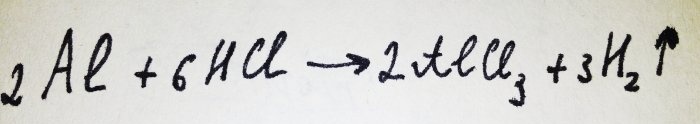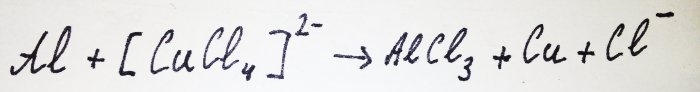Ennek lényege, hogy a reakció során felszabaduló hidrogén kék lánggal ég.
reagensek
Szüksége van tehát:
- Sósav-koncentráció 15%;
- Réz-szulfát;
- Alumínium fólia.
A kísérletet üvegedénybe végezzük.
Tartályként Petri-csészét vagy főzőpoharat készíthet. Nem javaslom a lombik használatát, mivel az utóbbi keskeny nyakának köszönhetően nehéz lesz az oxigén áramlása belül.
A kísérlet
A kísérlet elvégzése előtt határozottan javaslom, hogy ismerkedjen meg a savakkal végzett munka során alkalmazott biztonsági óvintézkedésekkel.
Öntsön egy üvegedénybe egy teáskanál vitriolt és öntsön 40 ml savat. Az oldat zöld színűvé válik a komplex rézion-tetraklorokuprát [CuCl4] 2 képződése miatt.
Most még csak hozzá kell adni az alumínium fóliát. Egy oxid-filmmel borítja, de a kapott komplex gyorsan elpusztítja. Ezután az alumínium egy része savval reagál, ennek a reakciónak az egyenlete:
Amint a reakcióból látható, hidrogén szabadul fel.
Az alumínium többi része kölcsönhatásba lép a komplexummal, kiszorítva a rézből:
A reakciók gyorsan megy végbe, nagy mennyiségű hő kibocsátásával.
A felszabadult hidrogén jól ég a levegőben, tegyük tüzet.
A szűk lángáramlás a doboz nyakának jellemzőivel jár, és az oldatban lévő rézionok telített kék színűek.
Tegyük ugyanazt a kísérletet, de egy másik tálban:
Amikor az összes alumínium reagál, az oldat szürkévé válik, és a felületen redukált réz foltok vannak. Bőv vízzel hígítani és a csatornába engedni.
Alján üledék található:
Azt is meg kell ártalmatlanítani, mivel a szűrés megkísérlése után egy világosbarna csapadék maradt a szűrőn, és ezt nem lehet réznek nevezni.
következtetés
És ebből a cikkből véget ért. Ezt az élményt az iskolai kémia órákon is be lehet mutatni. Sok szerencsét mindenkinek az ismétlésben!