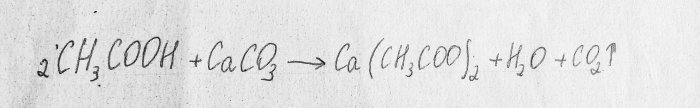Una part integral de qualsevol viatge llarg és una foguera. Els turistes solen utilitzar combustible sec per encendre ràpidament. Tanmateix, si un químic turista fa una caminada, hi ha alguna cosa més interessant: l’alcohol sòlid a l’arsenal per a l’encesa. Sembla així:
Es tractarà en aquest article. Tinc en compte que només el nom combina aquesta substància amb l’alcohol - ho comprovarem més endavant. Ara anem a coure-ho!
Necessitarà
Com a reactius químics utilitzarem el que es pot trobar fàcilment a les prestatgeries.
Per tant, per a la preparació d'alcohol sòlid necessitem:
- Àcid acètic 70%, venut en botigues de queviures;
- Tiza natural: en botigues d'una residència d'estiu;
- L’alcohol mèdic al 95% o l’alcohol isopropílic: en farmàcia o en una botiga de cotxes, respectivament.
També necessitem aigua i plats d’un sol ús (o productes químics) per a l’experiment i guants de goma. En cap cas, després d’acabar els experiments, no utilitzeu cap dels anteriors per menjar!
Com a tassa de mesura, podeu utilitzar una tassa de plàstic de 200 ml.
Comencem a fer alcohol sec
En primer lloc, afegir 60 ml d’àcid acètic i 125 ml d’aigua al matràs.
Ara afegim guix en porcions petites a la solució resultant. Les bombolles de gas comencen a destacar, mentre que és important agitar constantment la solució perquè tinguin temps d’esclatar.
El consum total de guix serà de 42 grams, però s’hauria d’afegir fins que no es dissolgui.
Considereu la reacció química del procés:
Es tracta d’una reacció de neutralització.
La primera substància és l’àcid acètic. El segon és el carbonat de calci, que es troba a la guix. El resultat d’aquesta reacció és el diòxid de carboni, l’aigua i l’acetat de calci. Aquesta substància és poc soluble en aigua, per tant, durant l'experiment, la solució pot endurir-se davant dels ulls:
En aquest cas, heu d’afegir una mica d’aigua i continuar l’experiment.
Quan l’àcid no roman a la solució, la reacció s’aturarà. Que quedi parat.
Passat algun temps, l’excés de guix s’establirà fins al fons, ja que per si mateix és insoluble en aigua. Ara filtra la solució:
He utilitzat un filtre de paper, també podeu utilitzar un coixinet de cotó.
La solució filtrada té una tonalitat groguenca, és una solució més o menys pura d'acetat de calci. Aboqueu una petita quantitat en un altre recipient i aboqueu-hi una mica d’alcohol. Comença a formar-se una massa similar a la gelea:
O una ombra més clara:
Enhorabona, ens vam endur l’alcohol dur. De fet, l’acetat de calci, a causa de la presència d’alcohol, que vam afegir, va començar a precipitar en forma de monohidrat; car l’alcohol tendeix a desplaçar les sals dels metalls divalents de la solució, que observem.
Ara amb les mans (sempre portem guants!) Donem a la nostra gelea la forma d’un cub o d’una bola.
A una temperatura de 160 graus centígrads, l’acetat de calci es descompon, en particular, en substàncies fàcilment combustibles, que contribueixen a la descomposició i suporten la flama.
Una peça d’aquesta mida pot cremar fins a sis minuts, cosa que és un resultat força bo. I dues peces són suficients per fer te per a una persona. Com a resultat de l’experiment, es va obtenir una quantitat suficient d’acetat de calci, cosa que significa que perdurarà molt temps.
Conclusió
Després de la fabricació, col·loquem l’alcohol sòlid de la forma requerida en un recipient hermèticament tancat i l’emportem amb audàcia en un viatge de càmping. I sobre això, aquest article va acabar. Que passeu bé!
P.S.També es poden cultivar cristalls incolors en forma d’agulla a partir d’acetat de calci, però aquesta és una història completament diferent ...