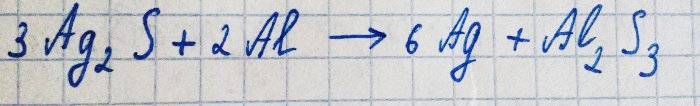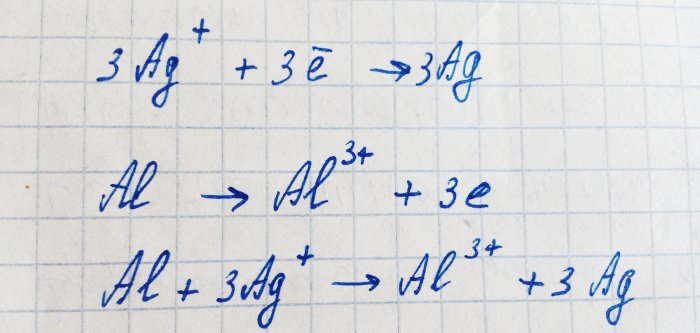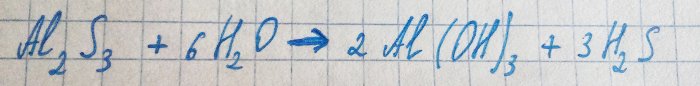Fa poc, em vaig posar a les mans un conjunt de coberts de plata que té aproximadament cent anys. Durant aquest temps, les culleres i ganivets van tenir temps d’enfosquir-se i embrutar-se, i vaig decidir netejar-los de la placa formada. En aquest article, compartiré una manera força efectiva amb la qual podeu retornar la brillantor antiga a la seva brillantor original. Així que anem.
Teoria
Primer, vegem per què la plata s’enfosqueix amb el pas del temps i d’on prové el rovell.
La plata (Ag) pràcticament no mostra reactivitat amb l’oxigen ni l’aigua, és a dir, no s’oxida. Aquesta propietat va ser notada per primer cop pels alquimistes, que van començar a anomenar plata un metall noble.
Tanmateix, l’argent reacciona amb sulfur d’hidrogen en presència d’oxigen. L’equació d’aquesta reacció és la següent:
El sulfur de plata resultant només cobreix el metall amb un film fosc, evitant que s’oxidi més.
Si els coberts no estan fets de plata pura (per exemple, 800 mostres), aleshores les impureses al rovell de l’aliatge.
Eliminació de l'oxidació
Preparem una solució d’àcid cítric. Com més saturat estigui, més ràpid i més ràpid es produirà la reacció. Col·loquem els coberts a l’interior quan les bombolles de gas deixin de sobresortir, les traiem de la solució, esbandim amb aigua i les netejem amb una tovallola de paper.
Per obtenir els millors resultats, podeu escalfar la solució a 80 ° C, i és important que es segueixin les mesures de seguretat.
Eliminació de la placa
Per eliminar la placa, utilitzem el mètode químic per reduir el sulfur de plata a un metall lliure.
Per això necessitem:
- - capacitat on es produirà la reacció;
- - refresc de bicarbonat;
- - paper d’alumini;
- - sal comestible;
- - aigua calenta.
Posem paper d’alumini a la part inferior del recipient, i objectes de plata amb el costat fosc a la part superior.
Aboqueu refresc per sobre.
Ara dissoldem la sal en aigua del càlcul: 6 cullerades senceres per litre d’aigua. Aboqueu la solució resultant al dipòsit, la reacció comença amb l’alliberament de sulfur d’hidrogen i diòxid de carboni.
Tot el procés s’ha de dur a terme al carrer, perquè el sulfur d’hidrogen té una olor característica d’ous podrits i és perjudicial per a la salut.
Mirem tota la química del que passa.
Inicialment, el sosa dissol una pel·lícula d’hidròxid prim de la superfície de la làmina.
Així, el sulfur de plata té l’oportunitat de reaccionar directament amb l’alumini.
L’alumini té una energia d’ionització inferior a la plata. S'oxida a un ió, donant plata als seus electrons. Aquest procés es pot escriure de la manera següent:
Aquesta reacció és electroquímica: a causa del moviment dels electrons de l’alumini a la plata, apareix una diferència de potencial.
La sal a la solució millora la seva conductivitat, permetent que la reacció continuï fins al final.
El sulfur d’alumini alliberat interactua immediatament amb l’aigua:
D'aquí el sulfur de hidrogen i l'olor corresponent.
Aquest procés pot trigar fins a mitja hora. Al final, cal rentar els coberts amb aigua i eixugar-lo amb una tovallola.
Després de la restauració de la plata, podeu utilitzar mitjans especials per conservar-la. Protegeixen la superfície de plata de la humitat i del sulfur d'hidrogen.
Així, l’argent conservarà el seu brillantor durant molt de temps.
Conclusió
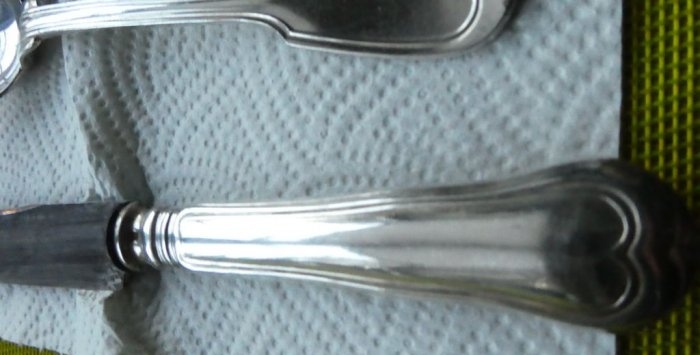
Fotos dels plats restaurats:
Com podeu veure, no hi ha rastre d’enfosquiment a les culleres. Els ganivets també van començar a estar millor, però, malauradament, part de la capa d’argent va desaparèixer de la seva superfície, tot i que es necessita el seu temps. Haureu de derivar-los a un especialista perquè torni a plata.
I sobre aquest article va arribar al seu final. Molta sort a tots en la repetició!