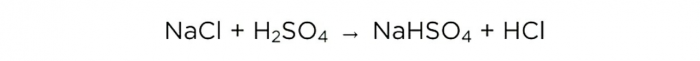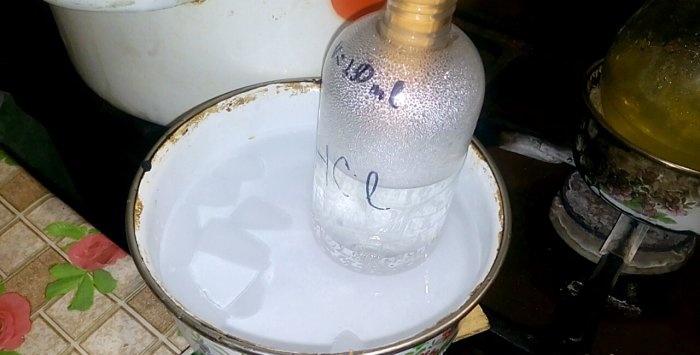Els alquimistes, que van rebre per primera vegada àcid clorhídric al segle XV, el van anomenar "spiritus salis", "esperit de sal". Aquest àcid tenia propietats màgiques en aquell moment: corroia paper, dissolia metalls, enverinava les persones. Aquestes propietats han romàs amb ella fins avui, però ara aquest àcid ha estat prou estudiat i no hi ha màgia aquí.
L’àcid clorhídric (HCl) és un àcid monobàsic fort, en la seva forma pura és un líquid clar. A la seva concentració màxima del 38%, "fuma" a l'aire. Rebrem un àcid amb una concentració a la meitat que.
Per tant, comencem
Precaucions de seguretat
Precaució, treballa amb substàncies tòxiques.
Tots els experiments s’han de dur a terme a una habitació ben ventilada o sota una caputxa de fum. Assegureu-vos de portar ulleres de seguretat (disponibles a la botiga. Botiga) i guants (si no trobeu guants químics especials, són de bona qualitat per rentar plats).
Al lloc de l’experiment, el bicarbonat ha d’estar present per tal de neutralitzar l’àcid en una situació no prevista (s’alliberarà diòxid de carboni i aigua).
Està totalment prohibit realitzar un experiment en contenidors metàl·lics.
Necessitarà
Per dur a terme l’experiment necessitarem:
- Electròlit àcid per a bateries (venut a la botiga de vehicles);
- Aigua destil·lada (ibid.);
- Sal (es troba a qualsevol cuina);
- Soda de cocció (vegeu les precaucions de seguretat).
Dels plats que necessiteu:
- Matràs de vidre;
- Un vas amb sorra on poder col·locar el matràs;
- Diverses tasses d’un sol ús de 200 ml;
Si teniu una bombeta resistent a la calor, podeu escalfar-la sota la flama oberta del cremador. Però tot i així ho recomano a través de sorra, en aquest cas absorbeix àcid.
També necessitareu un parell de cantonades de fontaneria amb un diàmetre de 50 mm i un cremador (en el meu cas, alcohol, però us recomano utilitzar-ne un de gas).
Etapa 1: evaporació
L’electròlit de la bateria és l’àcid sulfúric més 36% (H2SO4). Primer, hem d’augmentar la seva concentració.
Aboqueu 200 ml al got, és a dir, gairebé fins a les vores i aboqueu una mica més de la meitat del got al matràs. Feu un marcador amb un marcador i afegiu-ne la resta.
Vaig posar un reflector de paper al voltant del matràs per aconseguir un escalfament més eficient, però després el vaig eliminar perquè es va començar a fondre.
Ara posem el matràs al cremador i l’evaporem fins al nivell de la marca prèviament ajustada, fins i tot una mica més baixa.
Paral·lelament, posem la gasa plegada diverses vegades per la cantonada i la fixem amb una banda elàstica. Preparem una solució insaturada de soda i la submergim a l’extrem de la cantonada amb gasa.
Quan l’electròlit comença a bullir, posem un racó al matràs, s’asseu ben fort al damunt. L’extrem de la gasa s’envia a la finestra oberta.
Això és necessari si de sobte l’àcid sulfúric mateix comença a evaporar-se amb l’aigua. Si no escalfeu gaire el matràs, això no passarà.
Cremador en acció:
La potència del meu cremador és relativament petita, de manera que l’evaporació va trigar aproximadament una hora. Un cremador de gas o una estufa elèctrica acceleraria molt aquest procés.
Un cop acabada la primera etapa, una mica menys de la meitat de la solució hauria de romandre al matràs, és a dir, un àcid amb una concentració aproximada del 75%. No oblideu la precisió.
Deixeu-ho refredar a temperatura ambient.
Etapa 2: càlculs
Ara que tenim àcid sulfúric concentrat, podem dur a terme la reacció principal, queda així:
Però primer, fem alguns càlculs, i al final els comparem amb el que ha passat a la pràctica.
Així doncs, inicialment teníem 200 ml d’electròlits amb una densitat d’1,27 g / cm³. Observant la taula de densitats de l’àcid sulfúric, veiem que aquesta densitat correspon a una concentració del 36%. Calculeu el volum d’àcid:
200 ml * 36% = 72 ml - V (H2SO4)
Després d’evaporar la solució, la seva concentració i, en conseqüència, la densitat va augmentar. Mirem la mateixa taula i veiem que una concentració del 75% correspon a una densitat d’1,67 g / cm³.
Coneixent la densitat de corrent (p) i el volum (V) de l’àcid, esbrinem la massa:
m = p * V;
m (H2SO4) = 1,67g / cm³ * 72ml = 120g;
m (H2SO4) = 1,67g / cm³ * 72ml = 120g;
Ara de la química escolar recordem:
m (H2SO4) / M (H2SO4) = m (NaCl) / M (NaCl) = m (HCl) / M (HCl),
on M és la massa molar de la substància.
on M és la massa molar de la substància.
Les masses molars de H2SO4, NaCl i HCl són respectivament de 98, 58,5 i 36,5 g / mol. Ara podem esbrinar quanta sal es necessita i quina quantitat de HCl.
És a dir, necessitarem 72 g de NaCl, això és de 34 ml, en excés: un quart de tassa.
Excel·lent, i HCl en teoria serà de 44,7 g.
Hi ha una columna g / l a la taula de densitat de HCl. Prenem a partir d’aquí el valor per a la concentració del 15% - 166,4 g / l. El volum d’aigua necessari per obtenir un 15% de HCl és de 44,7 / 166,4,270 ml. Agafarem 200ml. Com a resultat, en teoria, obtindré un 22% d’àcid clorhídric.
Etapa 3: obtenció d’àcid
Connectem els dos racons de la manera següent:
I tota l'estructura serà així:
L’àcid corresponent es condensarà al vas amb l’etiqueta HCl, el volum d’aigua que hi ha és de 200 ml. Marqueu també el nivell de fluids actual d’aquest vas.
Retirem les cantonades i aboquem la quantitat de sal calculada en els càlculs al matràs a través de l’embut.
La solució es torna de color groc.
Perquè l’àcid clorhídric comenci a sobresortir, heu d’encendre el cremador. En primer lloc, lligem ben fort les cantonades al matràs i al recipient receptor.
Amb la condensació de l’àcid a l’aigua, es formen “ones verticals”. A més, la solució s’escalfa i s’ha de refrigerar. Per exemple, podeu posar un altre vas amb gel des de baix.
La reacció es produeix relativament ràpidament - 20 minuts després dels quals podeu apagar el foc. Donem els darrers parells d’àcid clorhídric per dissoldre’s a l’aigua, després que tanquem bé el recipient. Quan el matràs s’hagi refredat, diluïm la solució restant allà amb aigua (aproximadament a un) i l’abocem a la claveguera.
Resum
Amb l’etiqueta del vas, determinem quanta quantitat de líquid s’ha afegit. El tinc ⅙, és a dir, el 17%. Aquesta és la concentració del nostre àcid clorhídric. Compareu-ho amb l'obtingut en teoria.
El 17% / 22% * 100% = 77% és el rendiment de la reacció.
És important tenir en compte que no hi ha una sortida igual a 1, sempre hi ha pèrdues. En el meu cas, no és suficient l'electròlit evaporat. L’ideal seria que la concentració d’àcid sulfúric hauria de ser del 90-95%.
Comproveu la interacció amb l’àcid resultant.
Observem la ràpida evolució de l’hidrogen. Això significa que l’àcid és adequat per a experiments posteriors.
Variacions
Com a matràs, podeu utilitzar una ampolla de vidre neta de cervesa o soda, però sempre que la calefacció sigui el més suau possible. En comptes de cantonades de PVC, podeu agafar canonades de polipropilè i cantonades de diàmetre menor (adequades per al matràs).
Una vegada més, us insto a que observeu les precaucions de seguretat. Molta sort a tots!