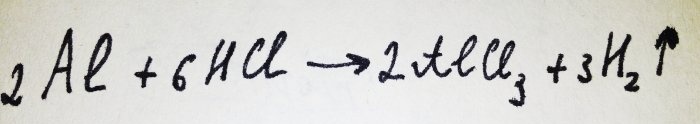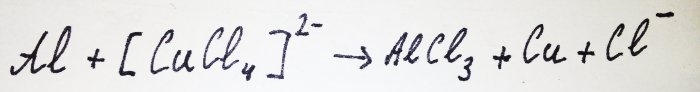Същността му е, че отделеният по време на реакцията водород гори със син пламък.
реагенти
Така че ние се нуждаем от:
- Концентрация на солна киселина 15%;
- Меден сулфат;
- Алуминиево фолио.
Експериментът ще се проведе в стъклен буркан.
Като съд можете да вземете чаша Петри или чаша. Не препоръчвам да използвате колбата, тъй като ще бъде трудно кислородът да потече вътре поради тясната шийка на последната.
експеримент
Преди да проведете този експеримент, горещо препоръчвам да се запознаете с мерките за безопасност при работа с киселини.
Изсипете в буркан чаена лъжичка витриол и изсипете 40 мл киселина. Разтворът става зелен в резултат на образуването на сложен меден йон тетрахлорокупрат [CuCl4] 2-.
Сега остава да добавите алуминиево фолио. Той е покрит с оксиден филм, но полученият комплекс бързо го унищожава. Тогава част от алуминия реагира с киселина, уравнението на тази реакция:
Както се вижда от реакцията, се отделя водород.
Останалата част от алуминия взаимодейства с комплекса, измествайки медта от него:
Реакциите протичат бързо, с отделяне на голямо количество топлина.
Освободеният водород гори добре във въздуха, нека го подпалим.
Тесният пламък се свързва с характеристиките на гърлото на консервата, а медните йони, които присъстват в разтвора, му придават наситен син цвят.
Нека направим същия експеримент, но в различна купа:
Когато целият алуминий реагира, разтворът става сив с петна от намалена мед по повърхността. Трябва да се разрежда с много вода и да се източва в канализацията.
В дъното има утайка:
Той също трябва да бъде изхвърлен, тъй като след опит за филтриране върху филтъра остана светлокафява утайка и не може да се нарече мед.
заключение
И по този начин тази статия приключи. Този опит може да бъде демонстриран в часовете по химия в училище. Успех на всички в повторението!